

1,项目概况
现有 xxx 公司的激光产品于 08/24/2020 被 FDA 列入 DWPE 名单。由于 改名单与海关进口警报联通,企业出口到美国的激光产品将被无条件扣留。 DWPE 为 Divisions may detain without physical examination 的简称,即 由于企业之前的违法行为被列入了 RED LIST,海关可在不经验证的情况下扣 留在改名单内企业的产品。 现需经过有效的方案,准备相关资料并与 FDA 进行申请和沟通,将企 业从 DWPE 中移除。
2,项目方案与计划
由于 DWPE 产生的原因是 FDA 核查到企业激光产品有违规的情况,并经 过通知后企业未进行进一步改善或解释,所以直接将企业列入了 red list。
所以,本次项目的服务内容将由如下步骤进行:
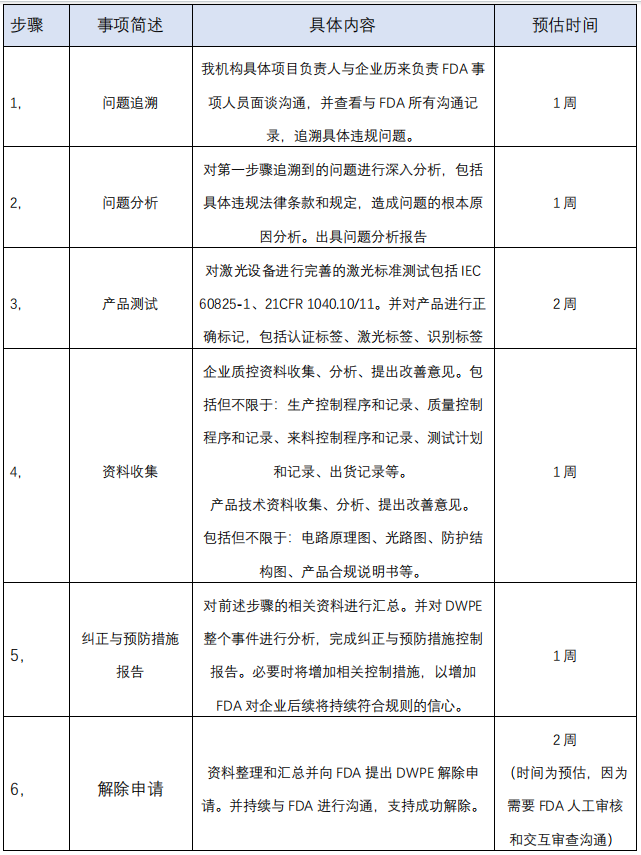
1, 与企业历来进行 FDA 认证注册的人员进行沟通,查阅与 FDA 往来 的所有相关信息,追溯具体违规事项。
2, 对违规事项进行深入分析,包括但不限于造成问题的原因,原因可 改善空间分析等。
3, 对产品进行完善的激光标准测试,并确保测试结果合格。
4, 从新对企业资料和产品技术资料进行收集(必要是问题改善),包 括但不限于:生产质量控制资料、检测和出货记录、产品技术资料 等各方面。
5, 对上述的分析、测试、生产和技术资料进行汇总。与第一条追溯到 的违规问题对应,编制完整的纠正措施与预防控制报告。
6, 开始与 FDA 沟通,申请解除 DWPE。
7, FDA 可能提出改善和分析资料的补正要求,依据 FDA 要求进一步 进行补充。
8, 解除 DWPE。
3,服务内容和时间计划

返回顶部